clonage
(de clone)

Obtention, par des manipulations biologiques, d’un ou plusieurs organismes – unicellulaires (bactéries, protistes) ou pluricellulaires (animaux, plantes) – génétiquement identiques entre eux et à l’organisme « modèle ».
Clonage moléculaire : technique de génie génétique permettant d’isoler et de multiplier des fragments d’ADN. Voir : clonage moléculaire.

La notion de clonage recouvre un ensemble de techniques permettant d'obtenir la réplication à l'identique d'une cellule ou d'un organisme, par multiplication végétative ou asexuée. La population ainsi obtenue, constituée de cellules ou d'organismes possédant tous le même patrimoine génétique, forme un clone. Chacun des éléments constitutifs de cette population peut être lui même qualifié de clone.
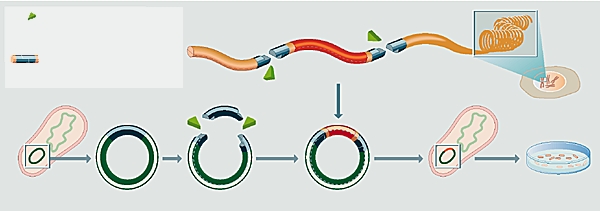
Il permet, par exemple, d'obtenir un grand nombre de bactéries possédant toutes un gène particulier que l'on veut étudier.
1. Dates clés du clonage
| DATES CLÉS DU CLONAGE | |
Clonage de cellules ou d'individus | |
| A. Carrel ; culture de cellules animales. | |
| Culture de cellules végétales. | |
| R. Briggs, T. King ; transfert de noyau à partir de cellules embryonnaires (têtard) chez la grenouille. | |
| J. Gurdon ; transfert de noyau à partir de cellules différenciées (intestinales) chez le crapaud. | |
| J. Gurdon ; premier clone viable de crapaud. | |
| S. Willadsen ; agneaux jumeaux obtenus par scission d'embryon. | |
| S. Willadsen ; clones d'agneaux par transfert de cellules embryonnaires. | |
| J. Hall, R. Stillman ; début de clonage humain par scission d'embryon non viable. | |
| I. Wilmut, K. Campbell ; premier clone de brebis adulte (Dolly), par transfert de cellule différenciée dans un ovocyte. | |
| Clones de singes par transfert de cellules embryonnaires dans un ovocyte. | |
| Premier clone humain obtenu par transfert de noyau d'une cellule de peau dans un ovocyte de vache. Expérience stoppée au 12e jour. | |
Clonage de gène | |
| J. D. Watson, F. Crick ; structure tridimensionnelle de l'ADN. | |
| Découverte des premières enzymes de restriction. | |
| S. Cohen, H. Boyer ; fusion de l'ADN de deux espèces de bactéries : première manipulation génétique. | |
| Première bactérie transgénique (produisant une protéine humaine). | |
| Premier mammifère transgénique (souris). | |
| Première plante transgénique (tabac). | |
| Porc transgénique. | |
| Vache transgénique. | |
| I. Wilmut ; premier clone transgénique (brebis Polly). | |
| Clones de veaux transgéniques. | |
2. Les techniques du clonage
2.1. La multiplication de cellules
Le clonage exploite deux des propriétés essentielles de la cellule : celle-ci mène une vie autonome et elle se reproduit (division cellulaire). Sur un milieu nutritif adapté, une seule cellule donne naissance à des millions de cellules identiques. En quelques heures on obtient un clone.
Dès le début du xxe s., des cultures de tissus d'animaux et de végétaux ont été tentées. La culture de peau humaine est aujourd'hui pratiquement maîtrisée. On sait aussi reconstituer un plant végétal entier à partir de quelques cellules isolées (les végétaux ont eux-mêmes la propriété de se reproduire par multiplication végétative, qui produit des végétaux tous identiques – de fait des clones). Cette multiplication végétative in vitro, la micropropagation, se substitue au bouturage traditionnel. Ainsi une seule plante (légume, arbre fruitier, essence forestière) peut être reproduite à des milliers d'exemplaires.
2.2. La scission de cellules embryonnaires
L'animal peut aussi être cloné. Les vrais jumeaux sont issus d'une seule cellule-œuf (l'ovocyte fécondé) qui s'est divisée en deux. In vitro, en scindant artificiellement une cellule-œuf ou un embryon de quelques cellules, on obtient à volonté des jumeaux. Cette technique, le clonage par scission de cellules embryonnaires, est maîtrisée chez les mammifères depuis 1979. De fait, de nombreuses espèces ont été clonées de la sorte. Une équipe américaine a même cloné ainsi des embryons humains en 1993 (les 48 embryons « jumeaux » obtenus ont été détruits).
2.3. Le transfert de noyau
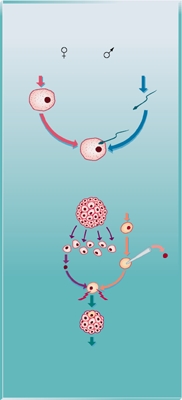
Cette technique de clonage a émergé de deux observations : d'une part, le noyau de n'importe quelle cellule d'un organisme contient toutes les instructions (tout le matériel génétique) nécessaires au développement complet d'un individu ; d'autre part, les premières générations de cellules issues de la division initiale de l'œuf sont indifférenciées et rigoureusement identiques (ce sont des cellules totipotentes, qui peuvent se différencier en n’importe quel type cellulaire ; différenciation cellulaire).
Il est donc possible d'obtenir un embryon, puis un individu, en remplaçant le noyau d'un ovocyte non fécondé par celui d'une de ces cellules indifférenciées. Le patrimoine génétique de l’individu qui se développe est identique à celui de l’embryon sur lequel on a prélevé le noyau. Ce mode de clonage a d'abord été expérimenté sur des crapauds à partir de 1952, et réussi pour les mammifères en 1985.
Une technique dérivée consiste à injecter dans l’ovule énucléé non pas le noyau d’une cellule embryonnaire, mais le noyau d’une cellule adulte, différenciée (c’est-à-dire une cellule qui n’exprime qu’une partie des gènes de son patrimoine ; par exemple une cellule de peau). Une fois dans l’ovule, le génome complet du noyau est en quelque sorte réactivé. L’individu qui se développe est identique à l’individu adulte sur lequel on a prélevé le noyau. Le premier mammifère cloné par transfert d’un noyau adulte (en l’occurrence issu d’une glande mammaire) est la brebis Dolly, née en 1996. En 1998, Dolly a mis au monde une agnelle, montrant que de tels clones sont non seulement viables, mais aussi féconds.
La technique est cependant associée à un risque élevé de fausses couches, de malformations, de mort prématurée. En fait, quelques pourcents seulement des embryons réimplantés sur des femelles porteuses produisent des individus viables et en bonne santé. De plus, si une cellule différenciée, prélevée sur un adulte, peut effectivement être reprogrammée pour donner naissance à un nouvel individu, ses chromosomes n'en ont pas moins subi un processus de vieillissement inexorable. Cela a été montré pour la première fois chez Dolly : elle était victime d’un vieillissement précoce, son âge réel ne correspondant pas à son âge apparent (le nombre d’années depuis sa naissance), mais à celui de sa « sœur » (la brebis adulte donneuse de noyau).
Le transfert de noyau de cellule adulte somatique (non reproductrice) a, depuis Dolly, été appliqué avec succès notamment à la vache, au cochon, au chat, au lapin, au mulet (l’équidé), à la souris et au chien. Il a aussi été utilisé chez un primate (le macaque), mais au cours de ces expériences (dont les résultats ont été publiés en 2007), aucun embryon ne s’est développé jusqu’à son terme. Une équipe japonaise est également parvenue à cloner des souris congelées (dont une depuis 16 ans).
3. Clonage reproductif et clonage thérapeutique
3.1. Le clonage reproductif
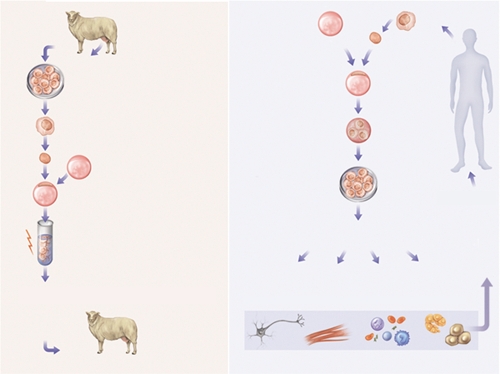
Le clonage reproductif consiste à produire de nouveaux individus tous identiques entre eux (des plantes comme des animaux). Il permet, en recherche fondamentale, d’étudier les mécanismes du développement. À l’avenir, il pourrait servir à produire des animaux d’élevage présentant tous des caractéristiques définies. Il pourrait aussi permettre de multiplier à l’identique des animaux transgéniques (OGM), produisant par exemple des médicaments (des facteurs de croissance ou de coagulation dans le lait de vaches, par exemple), sans que cette fonction puisse se perdre au cours d’une reproduction naturelle. On envisage aussi d’y avoir recours pour sauver des espèces animales menacées d’extinction ou, pourquoi pas, pour « ressusciter » des espèces disparues dont on possèderait l’ADN (mammouth congelé par exemple).
Le clonage reproductif, dans la perspective d’une application possible à l’homme dans le futur, soulève de nombreuses questions éthiques. Il a été déclaré « contraire à la dignité humaine » par l'Unesco, en 1997, dans la Déclaration universelle sur le génome humain et les droits de l'homme, adoptée par l'Assemblée générale des Nations unies, en 1998.
3.2. Le clonage thérapeutique
Le clonage à visée thérapeutique n’a pas pour but de créer de nouveaux individus, mais de disposer de cellules souches embryonnaires. Il utilise la technique de transfert d’un noyau dans un ovule énucléé ; le développement de l’embryon est ensuite stoppé au 5e jour. Les cellules souches embryonnaires sont alors cultivées et orientées vers la production de cellules spécialisées (cellules de peau, de tissu nerveux, de muscle, de foie, etc.). Le but de cette technique est de pouvoir ensuite introduire ces cellules en voie de spécialisation dans l'organe lésé d'un malade, pour induire une régénération du tissu déficient : muscle cardiaque en cas d'infarctus, cellules nerveuses en cas de maladies dégénératives (comme celles d'Alzheimer ou de Parkinson), pancréas en cas de diabète, etc. Le clonage thérapeutique en est encore au stade de la recherche.
4. La perspective du clonage humain : questions éthiques
La détection des anomalies génétiques et l'assistance médicale à la procréation (mères porteuses, bébés éprouvette fécondation in vitro, etc.) sont déjà globalement assimilées par la société. Le clonage humain à partir de cellules différenciées est maintenant techniquement possible, et a même commencé à faire l'objet d'expérimentations : le 25 novembre 2001, la société américaine d'ingénierie génétique ACT (Advanced Cell Technology) a annoncé la réalisation du premier clonage d'embryons humains à des fins thérapeutiques : trois embryons, obtenus par la même technique que celle ayant permis la naissance de la brebis Dolly, se sont développés pendant 72 heures, jusqu'au stade de 6 cellules. Les chercheurs ont justifié cette première par les perspectives hautement prometteuses de la médecine dite régénératrice, qui vise à utiliser des cellules souches embryonnaires humaines pour élaborer des tissus de rechange destinés à soigner certaines maladies (Alzheimer, Parkinson, cancer, diabète…).
Bien que les responsables de la firme américaine aient affirmé ne pas vouloir créer des êtres humains clonés mais seulement chercher à mettre au point des thérapies nouvelles, cette première scientifique a relancé le débat sur le clonage, beaucoup d'observateurs considérant qu'un pas de plus a été franchi vers le clonage à but reproductif, condamné par la quasi-totalité des instances nationales et internationales en charge des questions relatives à la bioéthique.
De plus, la technique elle-même de clonage thérapeutique pose question : quel doit être le statut de l’« embryon-médicament » fournissant les cellules curatives ? Doit-il être considéré comme un simple amas de cellules (son développement étant stoppé à un stade extrêmement précoce), ou comme un embryon destiné à devenir un être humain (ce qui serait le cas si on laissait son développement se poursuivre) ?
La perspective du clonage humain reproductif, dans la mesure où il donnerait naissance à des individus, soulève de nombreuses questions d’ordre moral (l’homme a-t-il le droit de jouer à l’apprenti sorcier, voire à Dieu, en fabriquant un être humain en-dehors des processus naturels de la reproduction ? La pratique du clonage reproductif est-elle dissociable de l’eugénisme ?) et philosophique (quelle liberté possède l’enfant physiquement identique à un adulte connu – son père ? sa mère ? –, à une frère ou une sœur décédé(e), à une « batterie » d’autres enfants ?).